Dysk międzykręgowy
Architektura hydrostatyczna a granice tolerancji obciążenia
Obszary: architektura dysku • ciśnienie śródjądrowe • dyfuzja • mechanotransdukcja • tolerancja obciążenia
Dlaczego architektura hydrostatyczna wymaga ruchu, a tolerancja obciążenia zaczyna się od metabolizmu
Dysk międzykręgowy jest strukturą aktywną. Jego budowa sprawia, że potrzebuje obciążenia, aby utrzymać równowagę biologiczną. Sposób podania siły – jej kierunek, czas trwania i rytm ruchu – decyduje o tym, czy tkanka będzie się adaptować, czy stopniowo tracić zdolność do regeneracji.
Współczesna analiza mechanobiologiczna redefiniuje dysk jako największy awaskularny organ w ciele człowieka – struktura pozbawiona bezpośredniego unaczynienia krwionośnego w której odżywianie komórek odbywa się wyłącznie drogą dyfuzji z naczyń sąsiednich trzonów kręgowych.
Ta unikalna cecha sprawia, że transport substancji odżywczych jest najważniejszym wyzwaniem klinicznym w prewencji i terapii dyskopatii. Każda interwencja terapeutyczna musi uwzględniać fakt, że komórki dysku operują na granicy wydolności metabolicznej, a ich los zależy niemal całkowicie od pasywnej dyfuzji przez blaszkę graniczną.
Dysk został zaprojektowany do pracy pod zmiennym obciążeniem. Zmienność ciśnienia podtrzymuje wymianę płynów i metabolizm komórkowy. Odpowiednio dawkowany ruch jest warunkiem adaptacji.
Architektura, która została zaprojektowana do przyjmowania obciążeń
Dysk składa się z trzech elementów: jądra miażdżystego (NP), pierścienia włóknistego (AF) oraz blaszek granicznych (CEP). Dzięki ich wzajemnej współpracy powstaje system zdolny do bezpiecznego przenoszenia obciążeń.
Bezpieczeństwo tego systemu wynika ze sprzężenia mechaniki z biochemią – siła mechaniczna musi zostać przekształcona w kontrolowaną odpowiedź komórkową. Na styku deformacji, ciśnienia i metabolizmu rozstrzyga się, czy obciążenie będzie zdrowym bodźcem anabolicznym, czy początkiem utraty tolerancji.
Cały model opiera się sprzężeniu czterech elementów:
- zdolności macierzy do wiązania wody i generowania ciśnienia,
- integralności sieci kolagenowej pierścienia włóknistego,
- drożności blaszek granicznych umożliwiających dyfuzję,
- zmienności obciążenia w czasie.
Każdy z tych elementów warunkuje stabilność całego układu. Utrata któregokolwiek zaburza równowagę między mechaniką a metabolizmem.
Modele biomechaniczne potwierdzają, że zaburzenie któregokolwiek z elementów – nawet przy zachowanej ogólnej wytrzymałości struktury – prowadzi do utraty symetrii rozkładu naprężeń i powstawania lokalnych stref przeciążenia [Ząbek 2025]. Architektura może pozostać makroskopowo stabilna, lecz funkcjonalnie pracuje już w warunkach nierównomiernego obciążenia.
Hydrostatyczny rdzeń: rola proteoglikanów w generowaniu ciśnienia
Pierwszym z elementów tej architektury jest zdolność jądra miażdżystego do wiązania wody i wytwarzania ciśnienia osmotycznego.
Za tę właściwość odpowiadają proteoglikany. Są to duże cząsteczki zbudowane z białka i łańcuchów cukrowych (glikozaminoglikanów), które wiążą wodę i wytwarzają ciśnienie osmotyczne w jądrze miażdżystym. Odpowiadają za jego zdolność do utrzymania uwodnienia i generowania oporu hydrostatycznego.
Jądro wiąże wodę i wytwarza ciśnienie osmotyczne. Pod wpływem kompresji osiowej wartość tego ciśnienia wzrasta. W ten sposób powstaje hydrostatyczny rdzeń zdolny do rozpraszania kompresji.
Wzrost ciśnienia zostaje przejęty przez pierścień włóknisty, którego włókna kolagenowe przekształcają kompresję w napięcie obwodowe (hoop stress). Dzięki temu siła rozkłada się równomiernie po obwodzie segmentu.
Integralność sieci kolagenowej pierścienia włóknistego warunkuje zakres i kierunek tej deformacji. Jeżeli struktura włókien traci spójność, napięcie obwodowe przestaje być równomierne, a część obszarów doświadcza większej lokalnej deformacji. W takich warunkach bodziec mechaniczny przestaje być jednorodny biologicznie. Jest to zjawisko fizjologiczne opisane w analizach mechanobiologicznych [Vadalà 2026].
Dynamika ciśnienia: ruch jako regulator środowiska
Opisany mechanizm dotyczy rozkładu sił w strukturze. Jednak architektura hydrostatyczna ujawnia swoje znaczenie dopiero w warunkach zmiennego obciążenia.
Ciśnienie w jądrze nie jest wartością stałą. Wraz z kompresją część wody opuszcza macierz, a w fazie odciążenia powraca. Ten cykl odkształcenia i rehydratacji podtrzymuje uwodnienie tkanki oraz umożliwia przemieszczanie rozpuszczonych cząsteczek.
Jeżeli kompresja utrzymuje się bez fazy odciążenia, przepływ płynu ulega ograniczeniu. Zmniejsza się porowatość macierzy, a dyfuzja substratów energetycznych staje się mniej efektywna. W tym momencie czas działania siły zaczyna mieć większe znaczenie niż jej wartość bezwzględna [Ząbek 2025].
Blaszka graniczna: wąskie gardło metabolizmu
Skuteczność cyklu kompresja–odciążenie nie zależy wyłącznie od przemieszczania płynu w obrębie jądra. Ostateczna wymiana substancji odżywczych wymaga ich przejścia przez blaszkę graniczną, która oddziela dysk od unaczynionych trzonów kręgowych.
Dysk pozostaje strukturą pozbawioną bezpośredniego unaczynienia. Tlen i glukoza docierają do komórek głównie drogą dyfuzji przez blaszkę graniczną [Tomaszewski 2015]. Oznacza to, że dostępność energii jest zależna zarówno od zmienności ciśnienia, jak i od przepuszczalności tej struktury.
Jeżeli kompresja utrzymuje się bez fazy odciążenia lub gdy mikroarchitektura blaszki ulega zmianie, transport substratów energetycznych zostaje ograniczony. W takich warunkach granica tolerancji przestaje być wyznaczana wyłącznie przez wytrzymałość kolagenu. Zaczyna zależeć od wydolności metabolicznej komórek.
Granice architektury: kiedy geometria staje się ograniczeniem
Zależność między geometrią a metabolizmem nie jest intuicyjna. Modele transportu pokazują, że zwiększenie wysokości dysku wydłuża drogę dyfuzji do centralnej części jądra. W pewnych warunkach może to prowadzić do spadku stężenia glukozy poniżej progu przeżywalności komórek [Gu 2026].
Mechanotransdukcja: jak komórka odczytuje środowisko obciążenia
Opisane wcześniej zjawiska – deformacja macierzy, zmienność ciśnienia oraz dostępność substratów energetycznych – definiują środowisko, w którym funkcjonują komórki dysku. To środowisko nie jest obojętne biologicznie. Każda zmiana kształtu macierzy i gradientów osmotycznych jest przekształcana w sygnał komórkowy.
Mechanotransdukcja stanowi proces, w którym bodziec mechaniczny zostaje przekształcony w odpowiedź biologiczną. Komórka nie reaguje na ciężar jako taki, lecz na sposób deformacji macierzy w czasie oraz na warunki metaboliczne, w których ta deformacja zachodzi.
W warunkach fizjologicznego obciążenia dynamicznego aktywowana jest synteza agrekanu i kolagenu typu II. Zmienność ciśnienia sprzyja utrzymaniu fenotypu anabolicznego. Natomiast przy przewlekłej kompresji statycznej lub ograniczonej dostępności energii uruchamiane są szlaki degradacyjne, w tym mechanizmy zależne od kanałów mechanosensytywnych, prowadzące do zaburzeń funkcji mitochondriów i apoptozy [Vadalà 2026].
W tym ujęciu tolerancja obciążenia nie jest wyłącznie właściwością strukturalną. Jest wynikiem zdolności komórki do adaptacyjnej odpowiedzi na warunki mechaniczne i metaboliczne.
Jeżeli tolerancja obciążenia jest efektem odpowiedzi komórkowej na środowisko mechaniczne i metaboliczne, interwencja terapeutyczna musi modelować to środowisko.
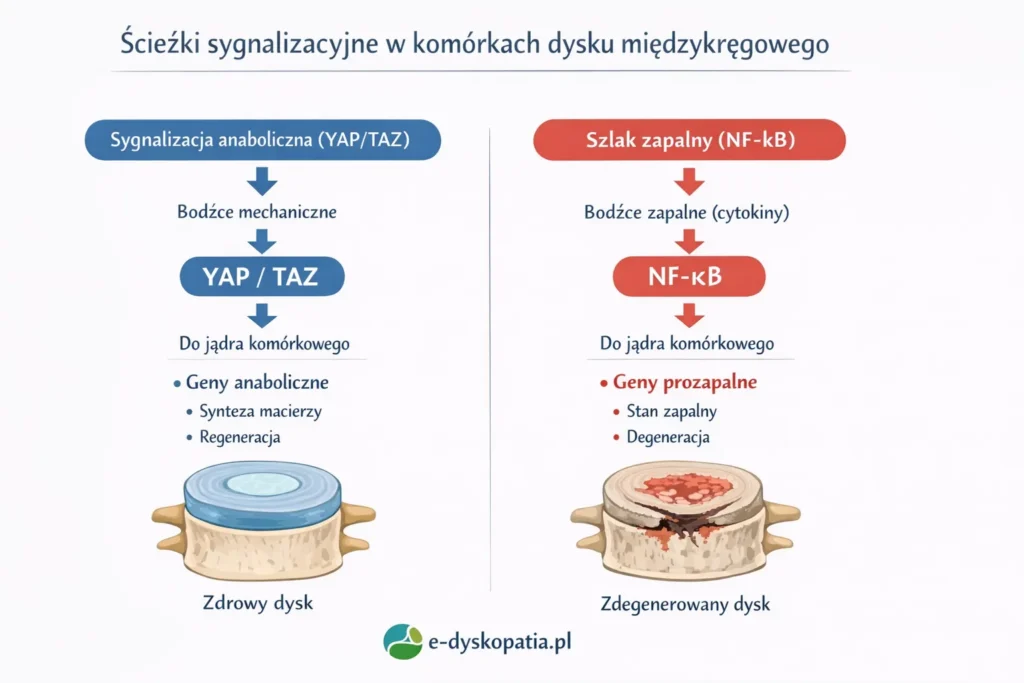
Komórka dysku nie reaguje na ciężar jako taki. Reaguje na sposób, w jaki macierz jest odkształcana w czasie. Zmienność obciążenia sprzyja anabolicznej odbudowie. Przewlekła statyka bez faz odciążenia przesuwa równowagę w kierunku degradacji.
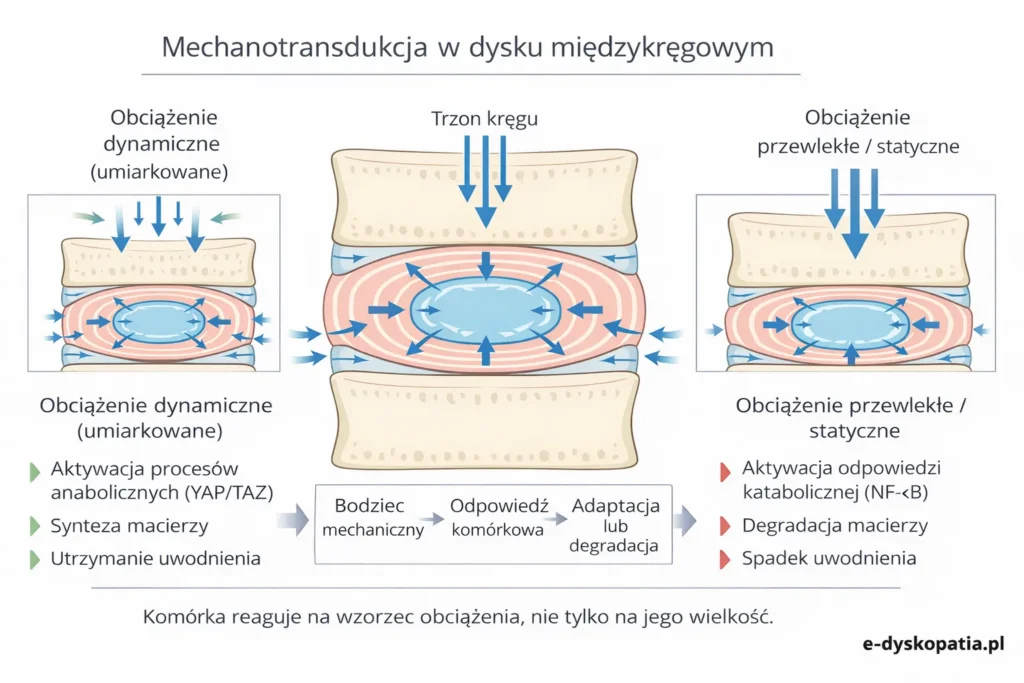
Jak to się przekłada na fizjoterapię
W terapii nie unikamy obciążenia. Modelujemy jego dawkę:
- stopniujemy ekspozycję na kompresję,
- wprowadzamy fazy odciążenia,
- kontrolujemy czas pozycji statycznych,
- budujemy tolerancję poprzez rytm i powtarzalność.
Architektura hydrostatyczna została zaprojektowana do pracy w warunkach zmiennego ciśnienia. To właśnie ta zmienność podtrzymuje zdolność adaptacji i zdrowy metabolizm.
Bibliografia
- Vadalà G. et al., 2026. Mechanobiology of Intervertebral Disc Degeneration: From Pathological Mechanisms to Therapeutic Approaches.
ResearchGate link - Ząbek Z. et al., 2025. Understanding the Microenvironment of Intervertebral Disc Degeneration: A Comprehensive Review of Pathophysiological Insights and Therapeutic Implications.
MDPI link - Tomaszewski K. et al., 2015. The biology behind the human intervertebral disc and its endplates.
Folia Morphologica link - Gu W. et al., 2026. Influence of disc height and strain-dependent solute diffusivity on nutrient transport in the human intervertebral disc.
PMC link